L’Agence européenne du médicament (EMA) recommande la suspension de l’autorisation de mise sur le marché de plusieurs agents de contraste linéaires. Ces préconisations, émises le 21 juillet 2017, confirment la position du comité d’évaluation des risques et de pharmacovigilance (PRAC) de l’EMA.
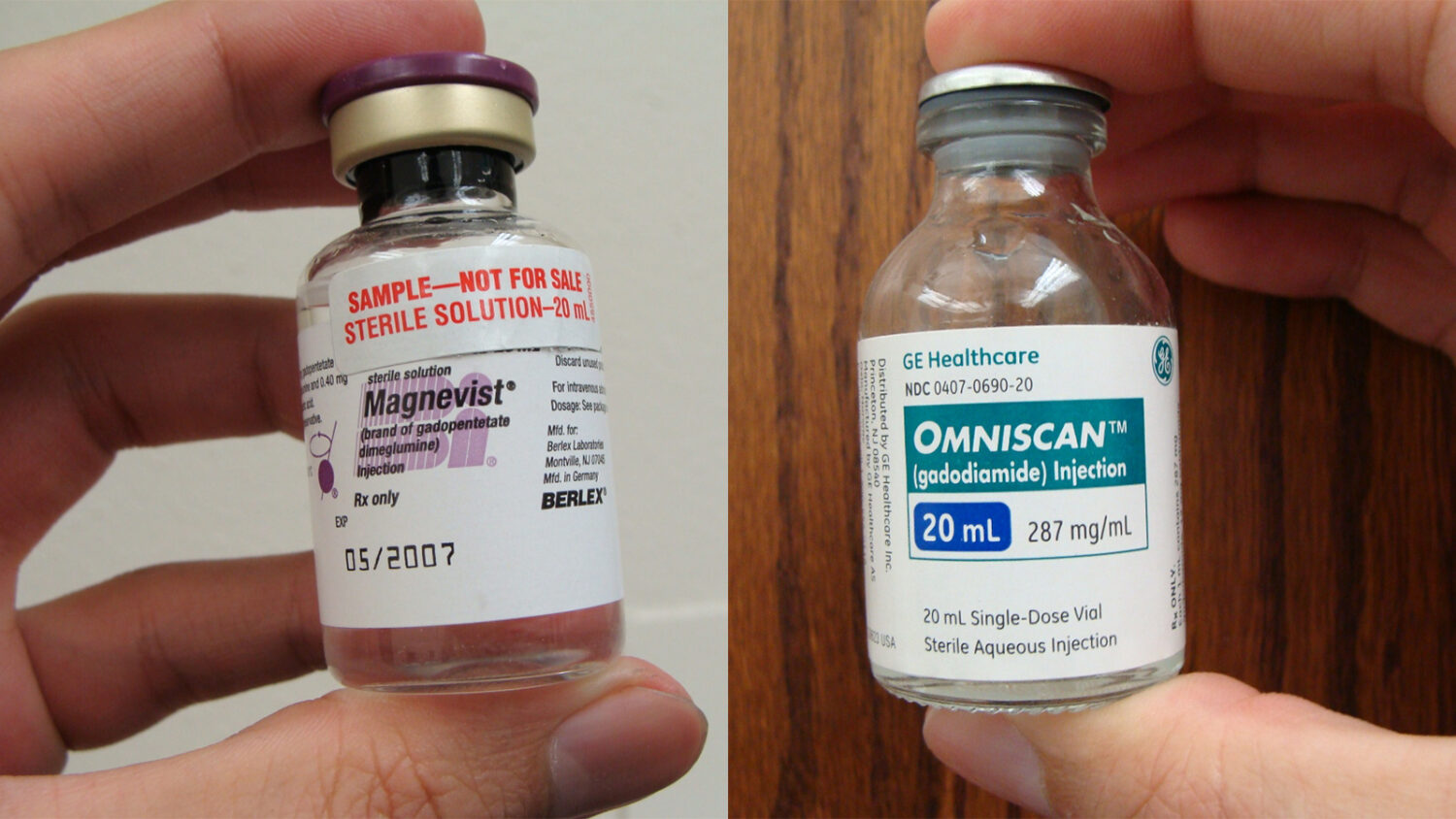
[contenu_encadre img= » » titre= »Les agents de contraste linéaires concernés par les recommandations » contenu= »gadopentétate dimeglumine (Magnevist®) : suspension de l’AMMacide gadobénique (MultiHance®) : restriction de l’AMM aux examens du foie
gadodiamide (Omniscan®) : suspension de l’AMM
gadoversetamide (Optimark®) : suspension de l’AMM » auteur= »B. B. » legende= » » credit= » »]
Preuve de l’existence de dépôts dans le cerveau
Dans un communiqué, L’EMA rappelle le pourquoi de ces recommandations : selon plusieurs études, des dépôts de gadolinium sont visibles dans le cerveau après l’injection de ces produits de contraste. Rien ne prouve qu’ils puissent causer un effet indésirable sur les patients, mais l’agence souhaite prévenir « tout risque » potentiel.
La Commission européenne décidera
La décision de l’EMA épargne les agents de contraste de type macrocyclique. Ces derniers « sont plus stables et présentent une propension plus faible aux dépôts de gadolinium », indique l’agence. Le dossier est maintenant sur les bureaux de la Commission européenne. Elle décidera – ou non – de suspendre officiellement ces autorisations de mise sur le marché.








Discussion
10 commentaires
Commenter cet article-

Docteur ImagoNous avons modifié la photo pour qu'elle soit plus représentative de l'article. #vilainsjournalistes
Il y a 9 ans
Signaler
-

Jérôme HoffErreur corrigée. Avec nos excuses.
Il y a 9 ans
Signaler
-

Line RenaudeauSauf que sur les photos on visualise des produits iodés et non du gado!!!
Il y a 9 ans
1 réponse
Signaler
-

Ludovic BordasAu second plan on voit du DOTAREM et du MULTIHANCE
Il y a 9 ans
Signaler
-

Paul MchlQuand on parle de gadolinium éviter de mettre en photos des produits iodées.... ^^'
Il y a 9 ans
5 réponses
Signaler
-

Thomas CampagneMon 'tit Paul'ochon, c'est précisé "photo d'illustration" ce qui veux dire "juste une tof histoire de faire genre, mais si c'est pas bon, bat les couilles frère" ?
Il y a 9 ans
Signaler
-

Paul MchlUn minimum de crédibilité tout de même..... Sur Google il ne manque pas de photos
Il y a 9 ans
Signaler
-

Thomas CampagneTu sais... Le journalisme aujourd'hui... Regarde les journalistes à la TV, soit disant l'élite... Comment ils bourdent... Alors sur le net avec des apprentis /débutants... ?
Il y a 9 ans
Signaler
-

Ludovic BordasAu second plan on voit du DOTAREM et du MULTIHANCE, c'est juste une illustration globale des produits de contraste en imagerie pour illustrer l'article... Ça n'enlève rien à la qualité de l'article ni au travail de documentation réalisé.
Il y a 9 ans
Signaler
-

Alice Ettaouir BertrandPas d'accord Ludovic Bordas, ils ne sont pas sérieux.
Il y a 9 ans
Signaler
Commenter cet article