Mardi 19 juillet 2016, 8 heures 15. Dans le département d’imagerie du CHU Dijon-Bourgogne, Annie Flamery et Mathilde Marchand, manipulatrices, consultent le dossier médical d’un patient avec les radiologues. Celui-ci est arrivé d’Auxerre hier pour bénéficier d’une cryothérapie rénale droite, dans le cadre du traitement d’une grosse tumeur rénale non opérable. L’hôpital François-Mitterrand est le seul établissement de la région Bourgogne Franche-Comté à pratiquer la cryoablation, une technique mise en place depuis quelques mois.
Les résultats des bilans biologiques sont satisfaisants. Les manipulatrices préparent la salle et le matériel. Elles cherchent du renfort pour apporter les bonbonnes d’hélium et d’argon stockées dans la salle attenante. Une tâche qu’elles devront réaliser tant qu’un branchement plus simple n’aura pas été prévu. Une fois mises en place, les bonbonnes sont testées et branchées sur la console mobile Visual Ice®. Cette dernière est mise en route. Les manipulatrices vérifient que rien n’a été oublié en consultant la fiche rédigée par Annie Flamery à l’époque de sa formation à la cryothérapie. Aujourd’hui, elle-même est chargée de former Mathilde Marchand, sa collègue.

Annie Flamery (à gauche) et Mathilde Marchand installent les bonbonnes d'hélium et d'argon qu'elles vont brancher sur la console de cryothérapie. © V. F.
Un patient sous diazanalgésie
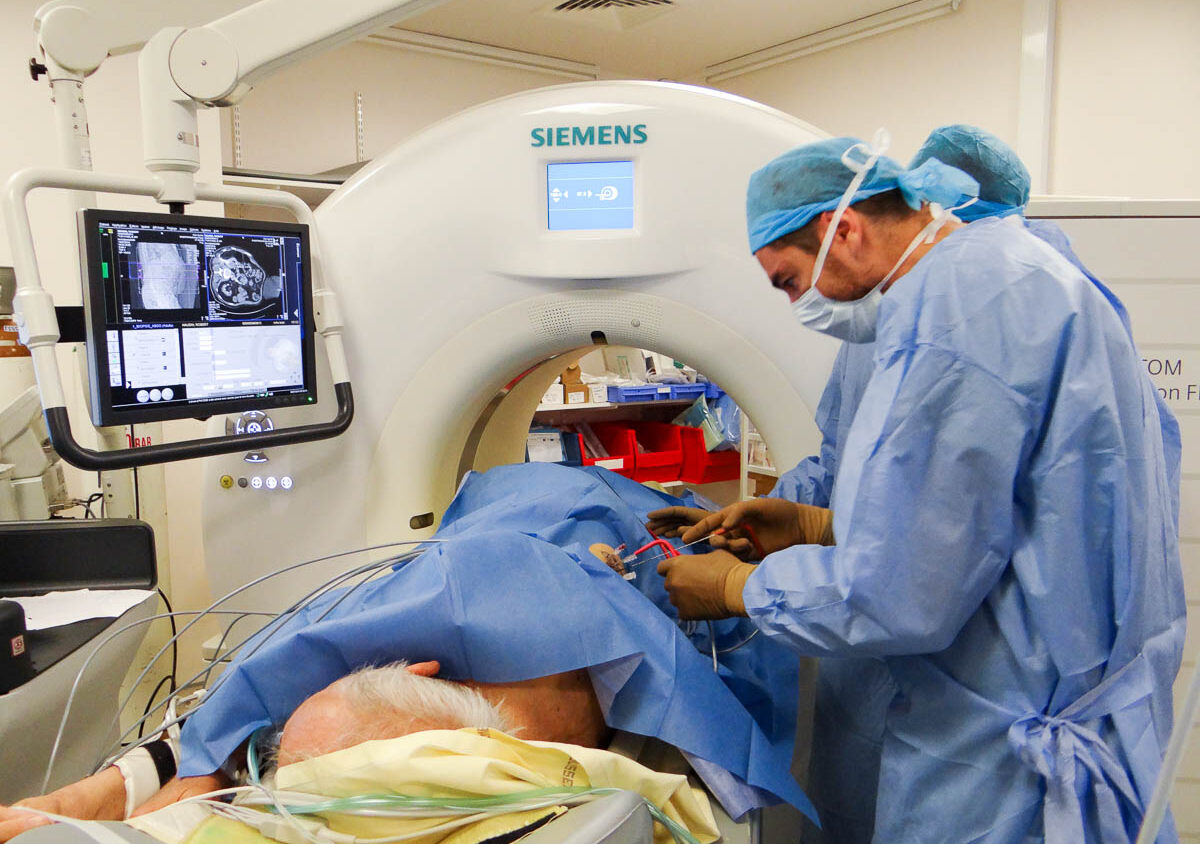
Le patient est installé avec le plus de confort possible sur la table du scanner. Des cales et moyens de contention lui sont proposés. Après quelques essais, le patient opte pour la position qui lui convient le mieux tout en respectant les besoins des radiologues. Le médecin anesthésiste, l’interne anesthésiste et l’infirmier anesthésiste le mettent sous diazanalgésie. Il est alors plongé dans un état de « sommeil » semi-conscient et ne ressent pas la douleur. Il n’a pas besoin d’être intubé.
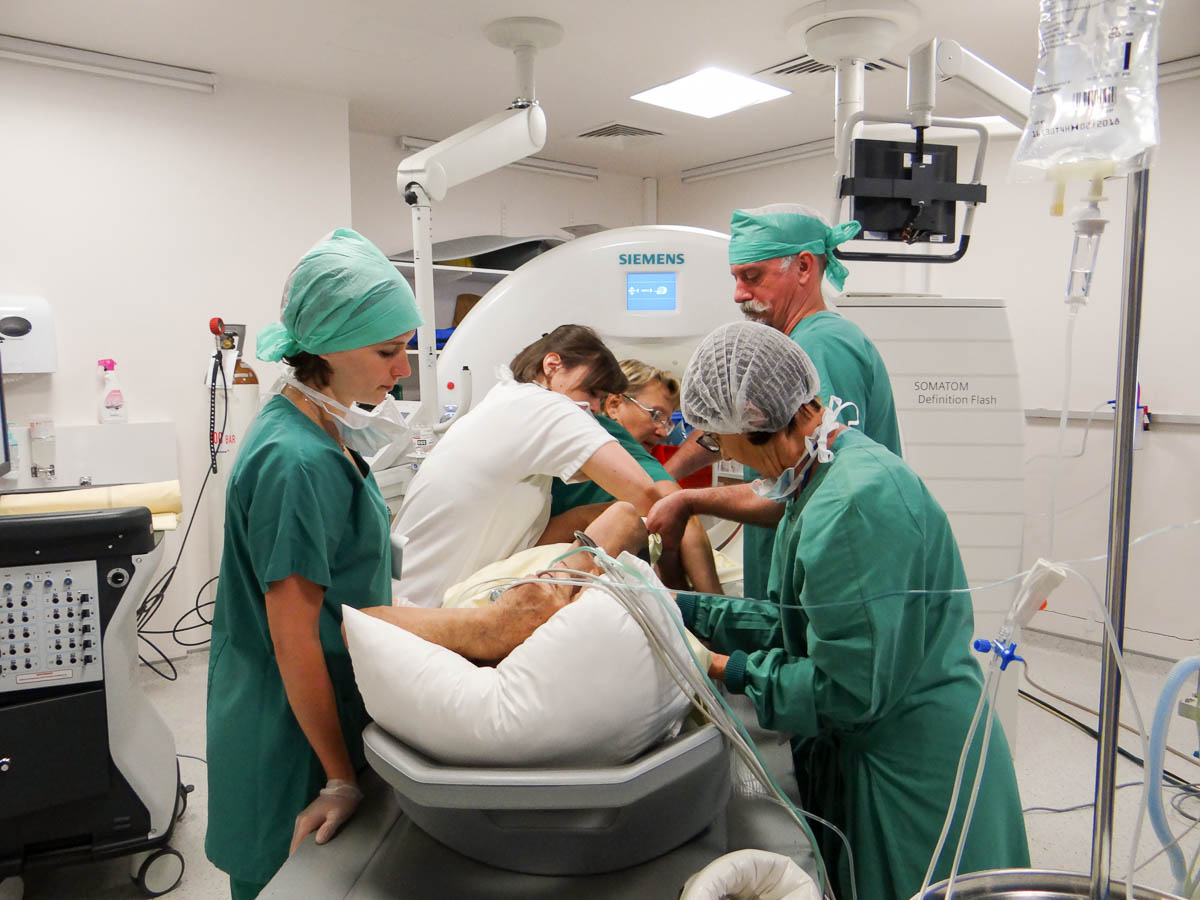
Le patient est installé avec le plus de confort possible, à l'aide de cales et de moyens de contention. © V. F.
Moins de risques pour les tissus voisins
Une première hélice de repérage est réalisée pour localiser La tumeur rénale. Pierre-Yves Genson, le radiologue chargé de la cryothérapie, demande ensuite un scanner avec injection. Une biopsie de la tumeur est prévue avant la cryothérapie. Vu la taille de la lésion, sept aiguilles Icerod® 1,5 CX seront nécessaires. « Nous allons devoir mettre 6 voire 7 aiguilles pour faire un gros glaçon. L’opération comporte trois phases : une phase de congélation, une décongélation, puis une recongélation, décrit Romaric Loffroy, le radiologue interventionnel qui supervise la procédure. L’avantage de cette technique est qu’elle permet de traiter de grosses lésions sous anesthésie locale. Nous pouvons aller très loin dans le sinus avec moins de risques que les autres techniques pour les structures avoisinantes, telles que les cavités pyélocalicielles. »
Sous l’œil du scanner
Les manipulatrices préparent la table stérile puis les aiguilles Icerod® 1,5 CX, avec l’aide des radiologues. Avant la désinfection de la peau, Annie reporte au feutre l’emplacement prévu des aiguilles sur le dos du patient.
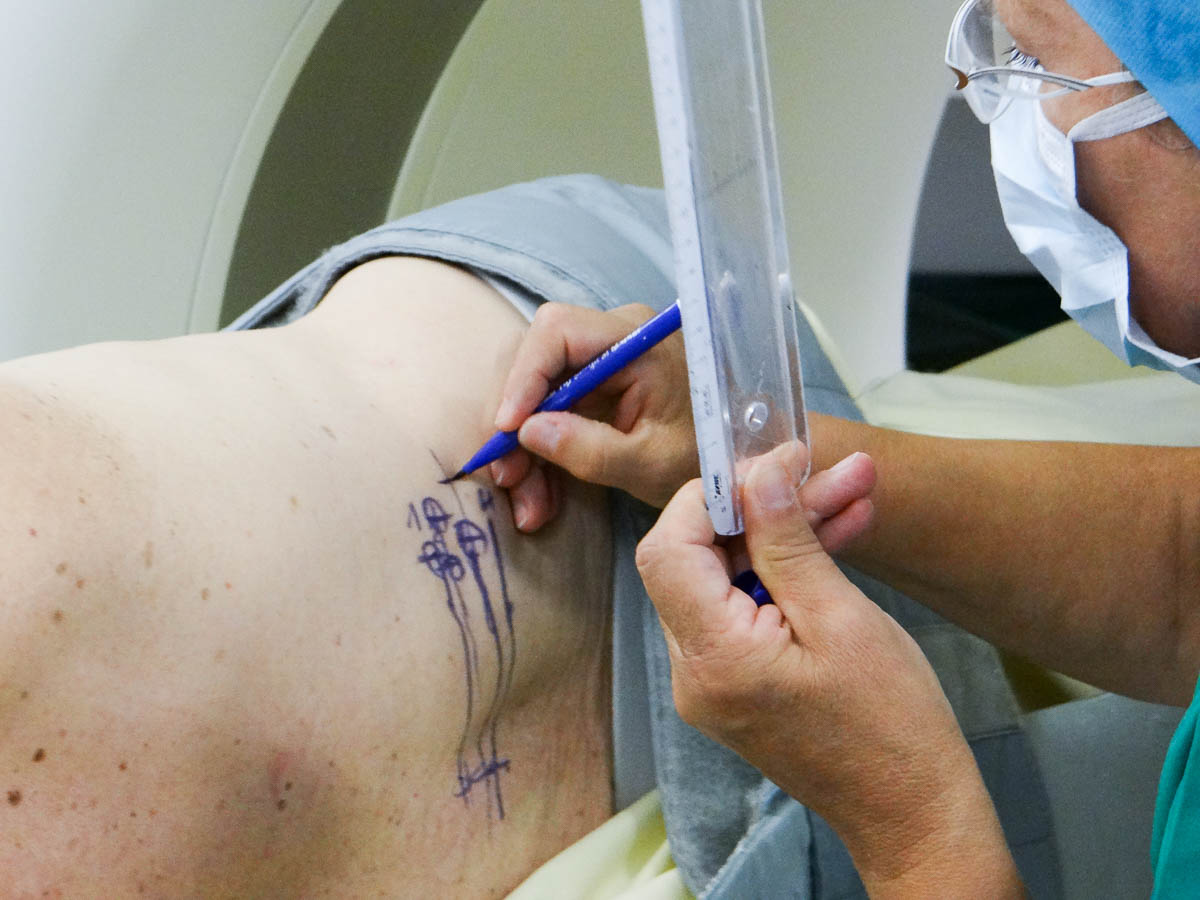
La manipulatrice marque les points d'entrée des aiguilles sur le dos du patient © Virginie Facquet
Le radiologue pratique une anesthésie locale puis ponctionne le rein pour déterminer la cytopathologie de la masse. « Des aiguilles à ponction lombaire sont ensuite posées pour préparer le trajet. Si elles sont bien placées, il ne reste plus qu’à les retirer et à prendre le même trajet avec l’aiguille de traitement. Elles servent juste de repérage », précise Sylvain Favelier, radiologue.
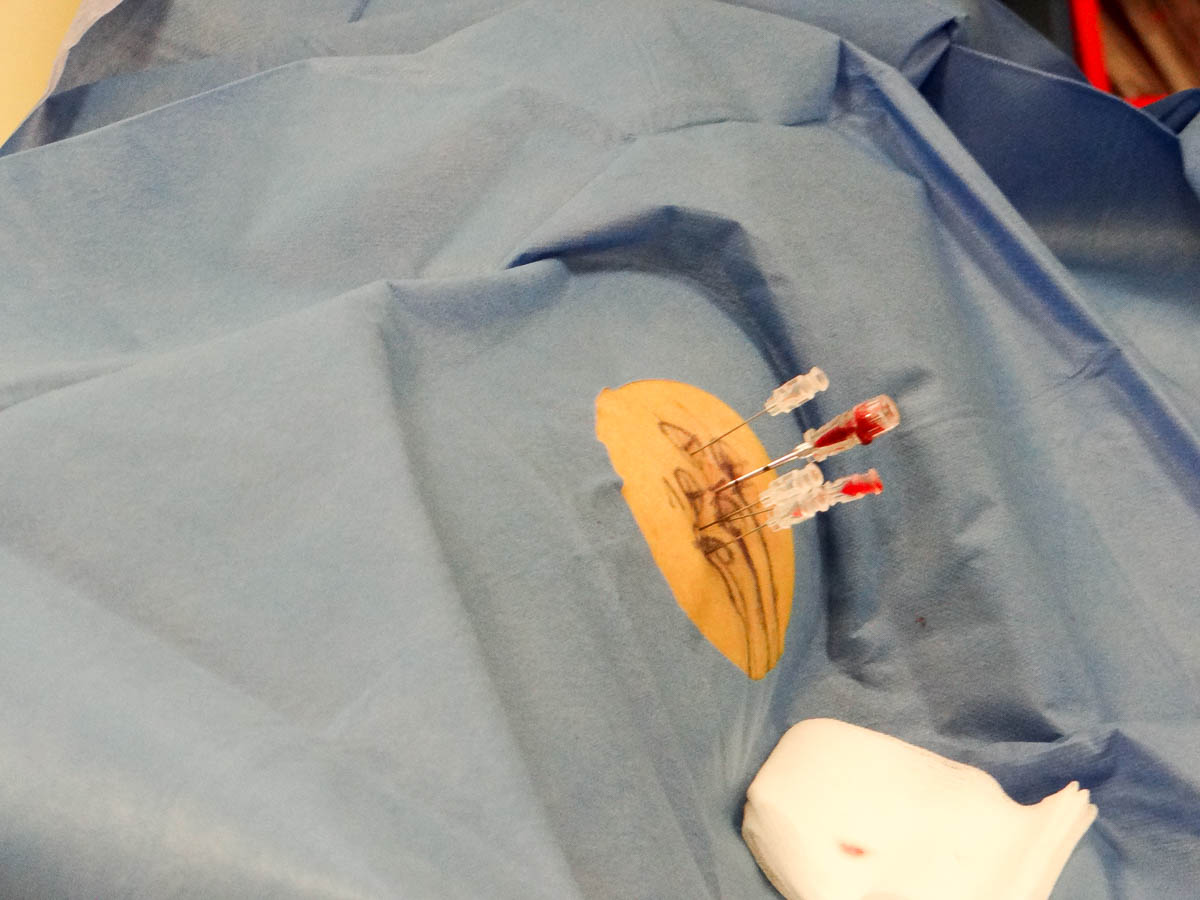
Le radiologue pose des aiguilles à ponction lombaire pour repérer l'endroit où placer les aiguilles de cryothérapie. © V. F.
Chaque aiguille de cryothérapie est branchée sur la console mobile et testée dans le sérum physiologique pour vérifier que toutes forment bien un glaçon. « Nous allons refaire une pile de coupes qui couvre l’ensemble du rein », annonce Annie Flamery. La première aiguille est fixée par congélation et des hélices de contrôle permettent de valider l’emplacement de chaque aiguille après sa pose. « La fenêtre est petite, cela n’irradie pas beaucoup le patient », souligne Mathilde Marchand.
Les aiguilles en synergie
Les images s’affichent sur l’écran de contrôle en salle de scanner pour que le radiologue puisse les visualiser. Une fois les aiguilles en place, Annie Flamery lance la phase de congélation. D’une durée de 10 minutes, elle est suivie par une phase de décongélation active de deux minutes. « La taille du glaçon varie en fonction du type d’aiguille. Quand nous plaçons plusieurs aiguilles, chacune produit un glaçon plus gros que si elle était seule. La destruction n’est pas proportionnelle au nombre d’aiguilles. Deux aiguilles détruisent comme s’il y en avait 3 », explique Pierre-Yves Genson.
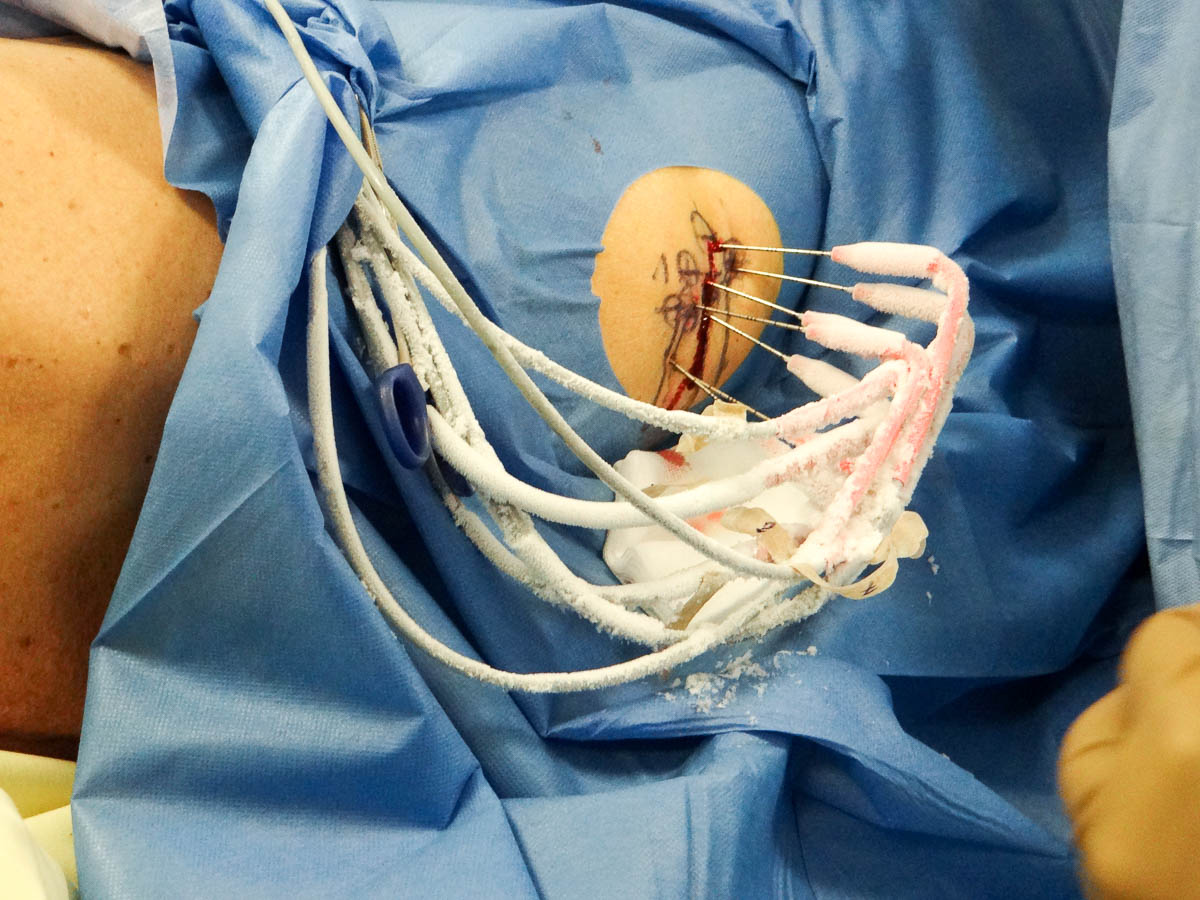
La première congélation dure 10 minutes. © V. F.
Destruction en deux temps
Après la décongélation, il faut changer la bouteille d’argon et relancer une phase de congélation de 8 minutes. Cette « recongélation » complète la destruction des cellules. « La première congélation entraîne une rupture des membranes cellulaires. La décongélation provoque un afflux d’eau dans les cellules. Le second glaçon est donc plus gros, tous les vaisseaux se détruisent et la tumeur se nécrose, expose Pierre-Yves Genson. Il existe aussi un effet retardé par ischémie tissulaire. » La cryothérapie, affirme le radiologue, a l’avantage de bien cibler la lésion : « La limite de entre zones traitée et non traitée est franche. L’épithélium qui supporte les cavités excrétrices n’est pas détruit par le froid alors que les techniques par le chaud comme la radiofréquence ou les micro-ondes détruisent les cavités, ce qui peut entraîner des complications. Les facteurs limitants sont la durée du geste et son coût », conclut-il. Le patient quitte l’hôpital deux heures plus tard. Un contrôle IRM sera réalisé dans 4 à 8 semaines pour s’assurer de la qualité du geste. « C’est toujours intéressant de pratiquer de nouvelles techniques. C’est valorisant, quoiqu’un peu stressant », témoigne Annie Flamery, qui se dépêche de poursuivre le programme de la matinée.










Discussion
Commenter cet article-

Guillaume VissioCette technique est aussi pratiquée depuis quelques années à l'Institut Mutualiste Montsouris.
Il y a 9 ans
Signaler
Commenter cet article