Encadrement de l'IA
Les outils d’IA marqués CE doivent contenir une déclaration d’utilisation prévue claire et complète
Afin d'assurer une utilisation sûre et conforme des dispositifs médicaux basés sur l’IA, les déclarations d'utilisation prévue des produits d'IA portant le marquage CE doivent contenir des informations complètes et compréhensibles avant que ceux-ci soient mis sur le marché. Pourtant, la majorité de ces déclarations manquent d’informations substantielles, selon une récente étude parue dans Insights into Imaging.
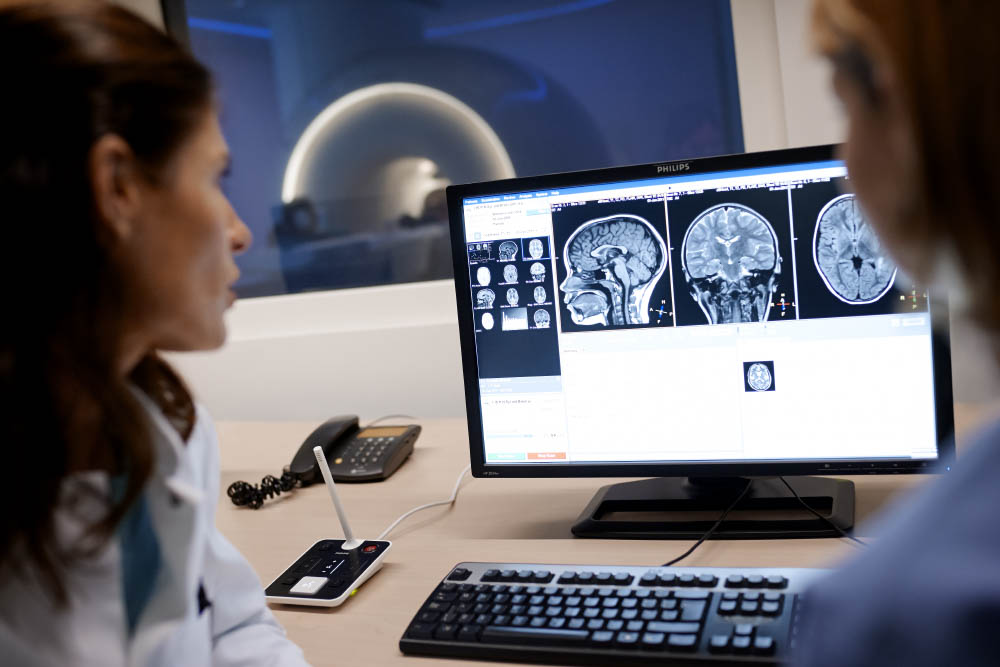
Les chercheurs ont analysé l’exhaustivité et l’ambiguïté des déclarations d’utilisation prévue des produits d’IA portant le marquage CE en radiologie par rapport aux exigences formulées dans les normes de la règlementation sur les dispositifs médicaux (photo illustration). D. R.
Il vous reste 76% de l’article à lire
Docteur Imago réserve cet article à ses abonnés
Vous avez déjà un compte ? Se connecter
- Tous les contenus « abonnés » en illimité
- Le journal numérique en avant-première
- Newsletters exclusives, club abonnés
Abonnez-vous !
Docteur Imago en illimité sur desktop, tablette, smartphone, une offre 100% numérique
23 €
par mois
Auteurs
Bibliographie
- Van Leeuwen K. G., Hedderich D. M., Harvey H. et al, « How AI should be used in radiology: assessing ambiguity and completeness of intended use statements of commercial AI products », Insights into Imaging, 16 février 2024. DOI : 10.1186/s13244-024-01616-9.







Discussion
Aucun commentaire
Commenter cet article