Les lésions vasculaires sont relativement prévalentes en population générale, touchant environ 1,5 % de la population. Elles peuvent être responsables d’une morbidité significative, de douleurs, d’inconfort et d’un préjudice esthétique qui peuvent réduire la qualité de vie [1]. Leur diagnostic est la plupart du temps clinique, mais l’imagerie a une place importante pour la confirmation diagnostique, nosologique, et pour les lésions complexes, à extension profonde, ou dans le cadre du bilan préopératoire [2].
Le lexique des anomalies vasculaires
Historiquement, le terme « angiome » était utilisé indistinctement pour dénommer plusieurs sous-types lésionnels, mais doit être abandonné du fait de son imprécision. La classification ISSVA (International Society of Study of Vascular Anomalies) est la plus fréquemment utilisée pour définir les types et sous-types de lésions vasculaires [3]. Elle est structurée autour des données cliniques, d’anamnèse, d’imagerie et histologiques. Cette classification divise schématiquement les anomalies vasculaires en 2 groupes : les tumeurs et les malformations. Parmi les malformations vasculaires, la première distinction nosologique clé se fait sur le flux intralésionnel, qui est bas pour les malformations veineuses (MV), capillaires (MC) et lymphatiques (ML) et élevé pour les malformations artérioveineuses (MAV) (figure 1).
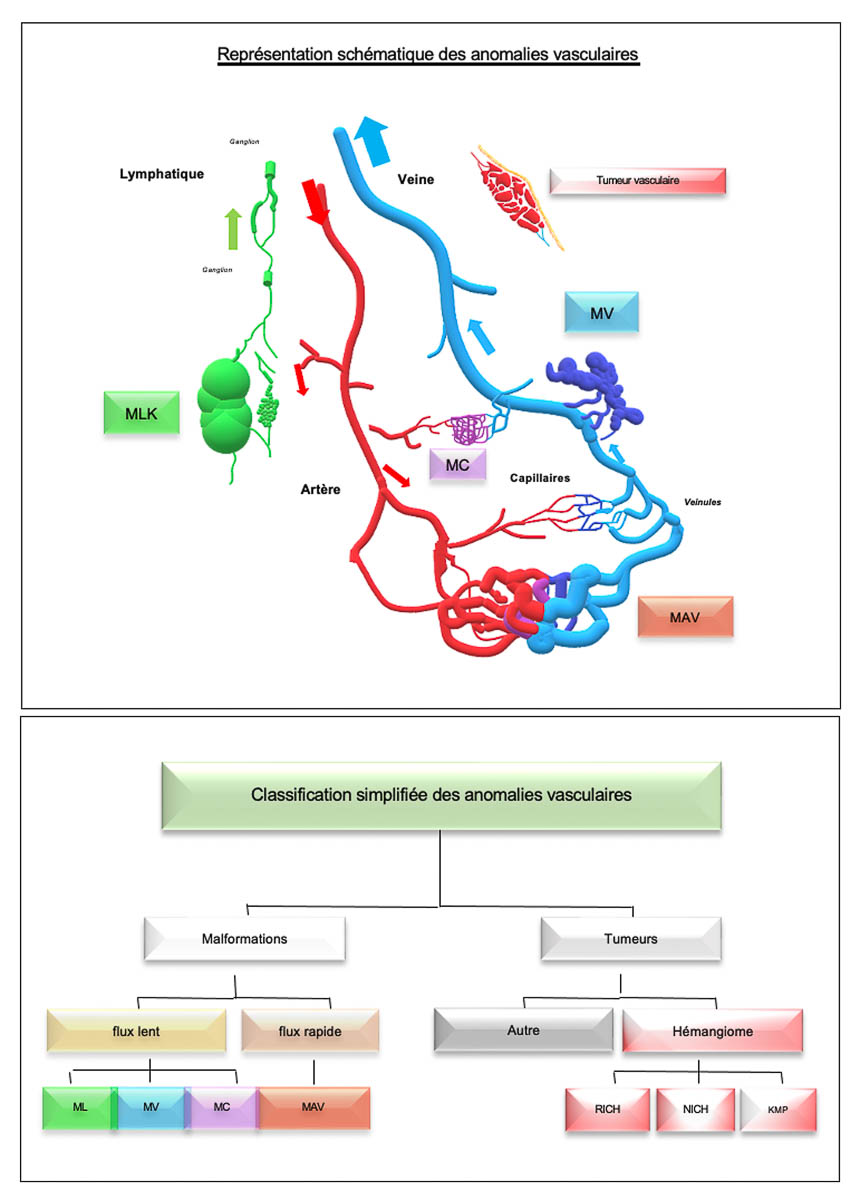
Figure 1. MC : Malformation capillaire ; MV : malformation veineuse ; ML : Malformation lymphatique ; MLK, ML kystique ; MAV : malformation arterioveineuse ; R-ICH / N-ICH Rapidly : non – involuting congenital hemangioma ; KMP : Kasabach Meritt Phenomenon. © Grégoire Boulouis, Denis Herbreteau
À l’inverse des tumeurs vasculaires, les lésions vasculaires malformatives ne sont pas caractérisées par une prolifération endothéliale mais par une anomalie structurelle, une dysfonction et/ou une surreprésentation de vaisseaux, sans prolifération cellulaire. Le sous-type de malformation est dénommé par le(s) contingent(s) vasculaire(s) le(s) plus représenté(s) (MV, ML, MC). Les malformations vasculaires complexes ou combinées regroupent plusieurs types de vaisseaux malformatifs (malformation veinolymphatique, malformation capilaroveineuse, etc.). La plus fréquente des tumeurs vasculaires est l’hémangiome infantile du nourrisson. Elle est rarement imagée car son diagnostic est clinique.
Il est important de noter que les malformations vasculaires sont déterminées génétiquement par des mutations somatiques [4] et qu’elles sont donc présentes dès la naissance (bien que leur évolution puisse les rendre symptomatiques / visibles plus tard dans la vie) (figure 2).
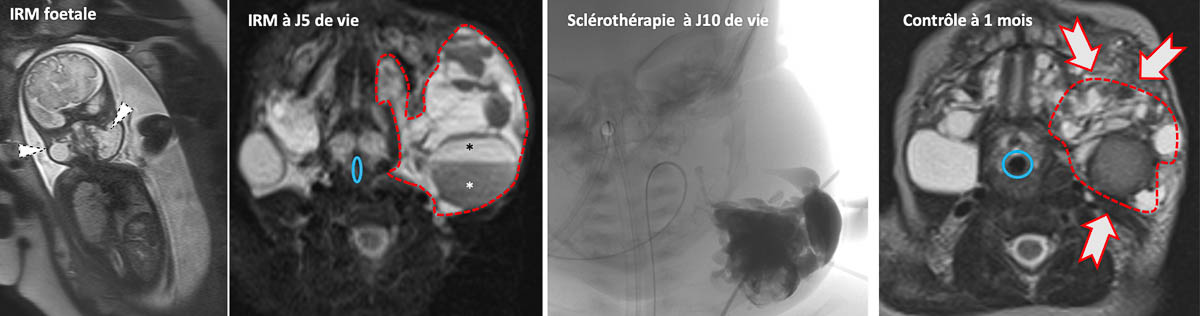
Figure 2. IRM fœtale (panneau de gauche), et imagerie postnatale chez un garçon porteur d’une malformation lymphatique kystique (MLK) macrokystique cervicale. À 5 jours de vie, l’IRM montre de volumineux « macro » kystes (zone tirets rouges) dont l’un présente des remaniements hémorragiques avec niveau liquide-liquide (astérisques). Une sclérothérapie a rapidement été réalisée, en raison de la compression engendrée par la MLK sur la filière aérienne (ovale bleu). À 1 mois, il y a une nette réduction du volume des kystes sclérosés, et une amélioration du calibre de la filière aérienne. © Grégoire Boulouis, Denis Herbreteau
Un diagnostic principalement clinique
L’examen clinique et l’anamnèse sont déterminants pour le diagnostic positif et nosologique des lésions vasculaires superficielles, premier argument pour des soins intégrés au sein de filières pluridisciplinaires et coordonnées en dermatologie. Le mode évolutif des lésions vasculaires est souvent une aide au diagnostic, car les MV et les ML évoluent typiquement par poussées évolutives inflammatoires, spontanément résolutives, ce qui n’est pas le cas des MAV et des tumeurs vasculaires.
Il est important de différencier rapidement les malformations à bas débit de celles à haut débit, qui ont un potentiel évolutif parfois sévère et pouvant mettre en jeu le pronostic fonctionnel ou vital. Ainsi, par extension de l’examen clinique, la disponibilité d’un appareil Doppler en consultation d’angiodysplasie est importante.
L’imagerie à visée préthérapeutique
Le bilan d’imagerie n’est pas systématique et se justifie en cas de doute diagnostique et à visée préthérapeutique pour caractériser l’extension en profondeur et les rapports anatomiques des lésions vasculaires. Le scanner et la radiographie standard n’ont qu’une place très secondaire dans le bilan d’imagerie, pour lequel l’échographie et l’IRM sont les modalités les plus utiles.
Pas d’imagerie pour les malformations capillaires
Les malformations capillaires sont des malformations hémodynamiquement inactives, intéressant les vaisseaux capillaires du derme. Leur couleur rose les différencie visuellement des malformations veineuses, ainsi que leur extension uniquement superficielle, « plane ». Aucune imagerie n’est réalisée pour les malformations capillaires. Elles peuvent être cependant le marqueur d’une pathologie plus complexe, comme les « faux angiomes plans » qui sont associés aux MAV au stade calme, et les malformations capillaires segmentaires qui peuvent être associés à différentes anomalies vasculaires syndromiques.
Échographie et IRM pour les malformations lymphatiques
Les malformations lymphatiques (ML) sont des anomalies de développement des vaisseaux primitifs lymphatiques qui peuvent être diagnostiquées en période anténatale, pour les lésions volumineuses (figure 2) [5]. Selon la taille des kystes, on distingue les ML macro- et micro- kystiques. Les formes macrokystiques se révèlent comme des masses rénitentes sous-cutanées, transilluminables. L’évolution se fait par poussées inflammatoires, en augmentant brutalement de volume et en devenant douloureux au cours d’épisodes infectieux ou d’hémorragies intrakystiques. Les formes microkystiques sont composées de vésicules translucides ou hémorragiques millimétriques sur une peau ou une muqueuse d’apparence normale, parfois responsables d’un épaississement cutané.
L’extension en profondeur et l’opportunité d’un traitement invasif sont évaluées par l’échographie et surtout par des séquences T2 fat sat en IRM (figure 2). L’injection de gadolinium n’est pas nécessaire mais peut montrer une prise de contraste uniquement des parois kystiques.
Les malformations veineuses ont un aspect IRM caractéristique
Les malformations veineuses sont des anomalies vasculaires ubiquitaires. Elles peuvent atteindre la peau, les tissus sous-cutanés, les muscles mais aussi les os. Ces masses ou nappes bleutées molles, gonflent en position déclive ou à l’effort et sont facilement vidées par la compression. Elles sont présentes dès la naissance, souvent de façon discrète, et deviennent visibles ou gênantes au fur et à mesure des années. Elles peuvent être accessibles à un traitement chirurgical ou à une sclérothérapie, pour laquelle la principale préoccupation sera de ne pas risquer de migration systémique de l’agent sclérosant. L’aspect IRM est caractéristique (figure 3) et la présence de phlébolithes permet de faire un diagnostic de certitude.
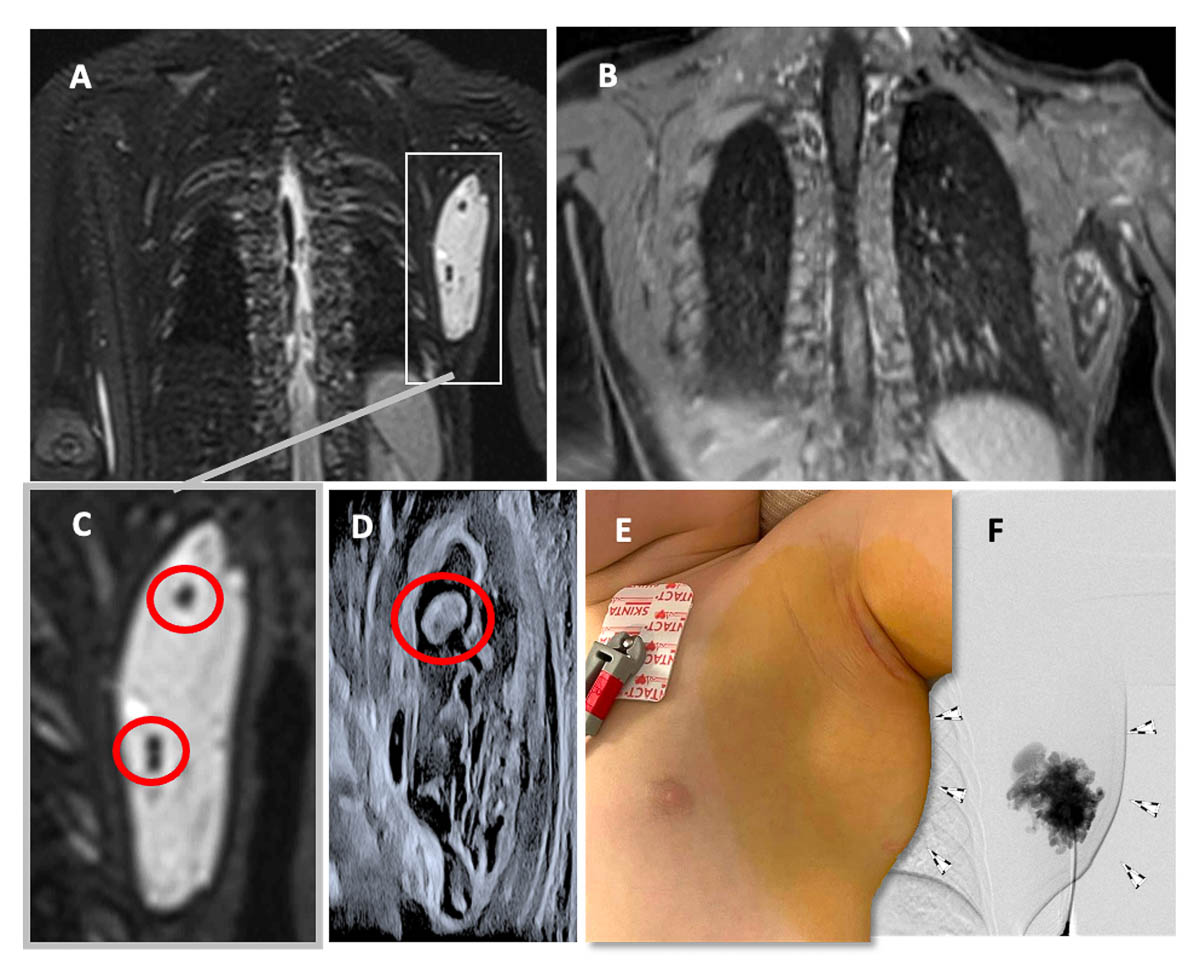
Figure 3. Malformation veineuse latérothoracique gauche chez un enfant d’1 an. Aspect caractéristique en T2 fat sat (A et C), avec lésion lobulée contenant des phlébolithes (cercles rouges), pathognomoniques sur les lésions à flux lents. Le rehaussement est hétérogène au temps précoce post injection témoignant du caractère peu vascularisé (B). L’aspect échographique est peu spécifique (D), mais retrouve les lobulations, et un phlébolithe. En E, l’aspect macroscopique avec voussure latérothoracique sans bleuissement cutané chez ce patient ou la lésion est sous-hypodermique. En F, aspect lobulé en phlébographie par ponction directe du contingent inférieur, avant injection d’agent sclérosant. © Grégoire Boulouis, Denis Herbreteau
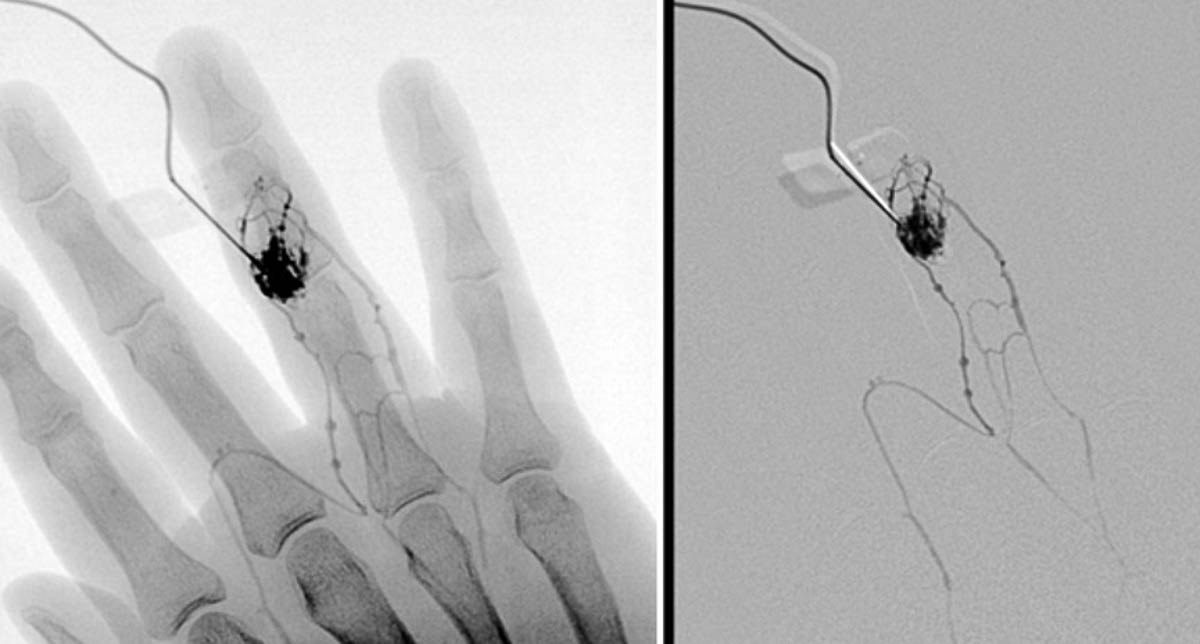
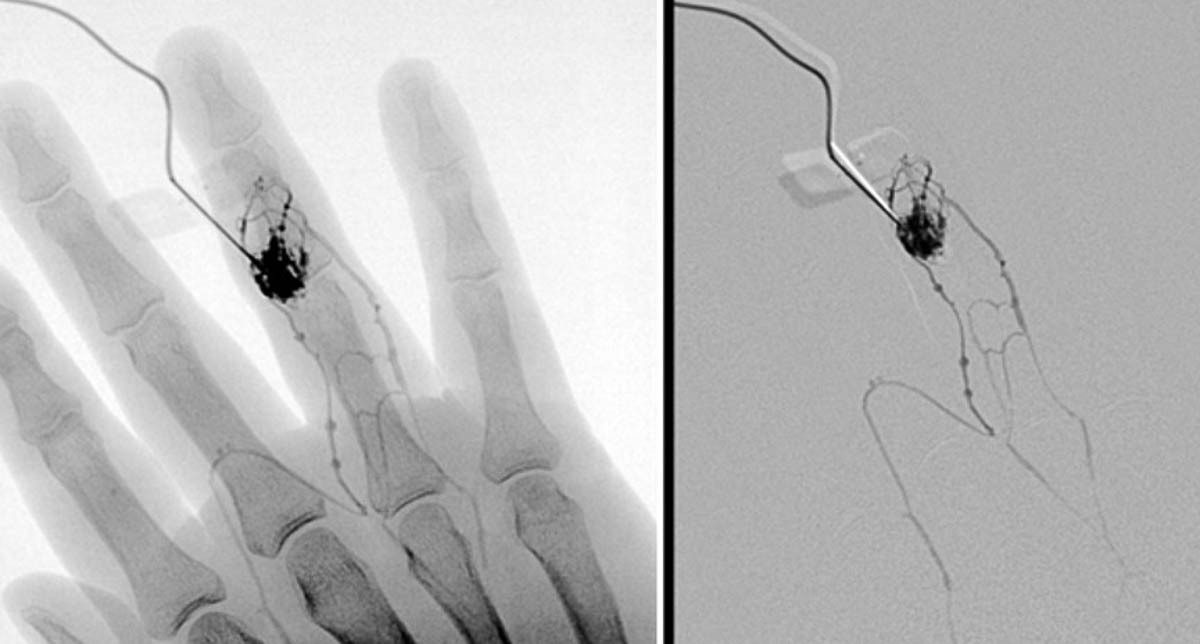
Figure 4. Aspect angiographique d’une malformation veineuse du 4e rayon de la main droite, sur une phlébographie réalisée avant sclérothérapie. On note la connexion au système veineux non malformatif, qu’il faut tarir avant injection de sclérosant. © Grégoire Boulouis, Denis Herbreteau
L’écho-Doppler et l’artériographie confirment le diagnostic de malformation artérioveineuse
Les malformations artérioveineuses sont beaucoup moins fréquentes et ont un potentiel morbide plus important. Évoluant par phases, elles peuvent rester quiescentes pendant de très longues périodes et évoluer ensuite de façon progressive ou brutale vers des formes actives qui sont localement destructrices (ulcérations, saignements), et peuvent mettre en jeu le pronostic vital et fonctionnel (insuffisance cardiaque, perte de fonction par destruction tissulaire, etc.) Elles ont une présentation très polymorphe : tuméfaction cutanée et sous-cutanée rouge ou violacée, parfois kératosique, chaude, pulsatile avec un souffle et parfois un thrill. Tout acte chirurgical ou endovasculaire, tout traumatisme et toute modification hormonale (puberté, grossesse, pilule) est susceptible de déclencher une poussée évolutive difficilement contrôlable. Les MAV doivent être prises en charge en centre spécialisé. Le diagnostic de MAV est suspecté cliniquement et confirmé par l’écho-Doppler puis par l’artériographie (figure 5).
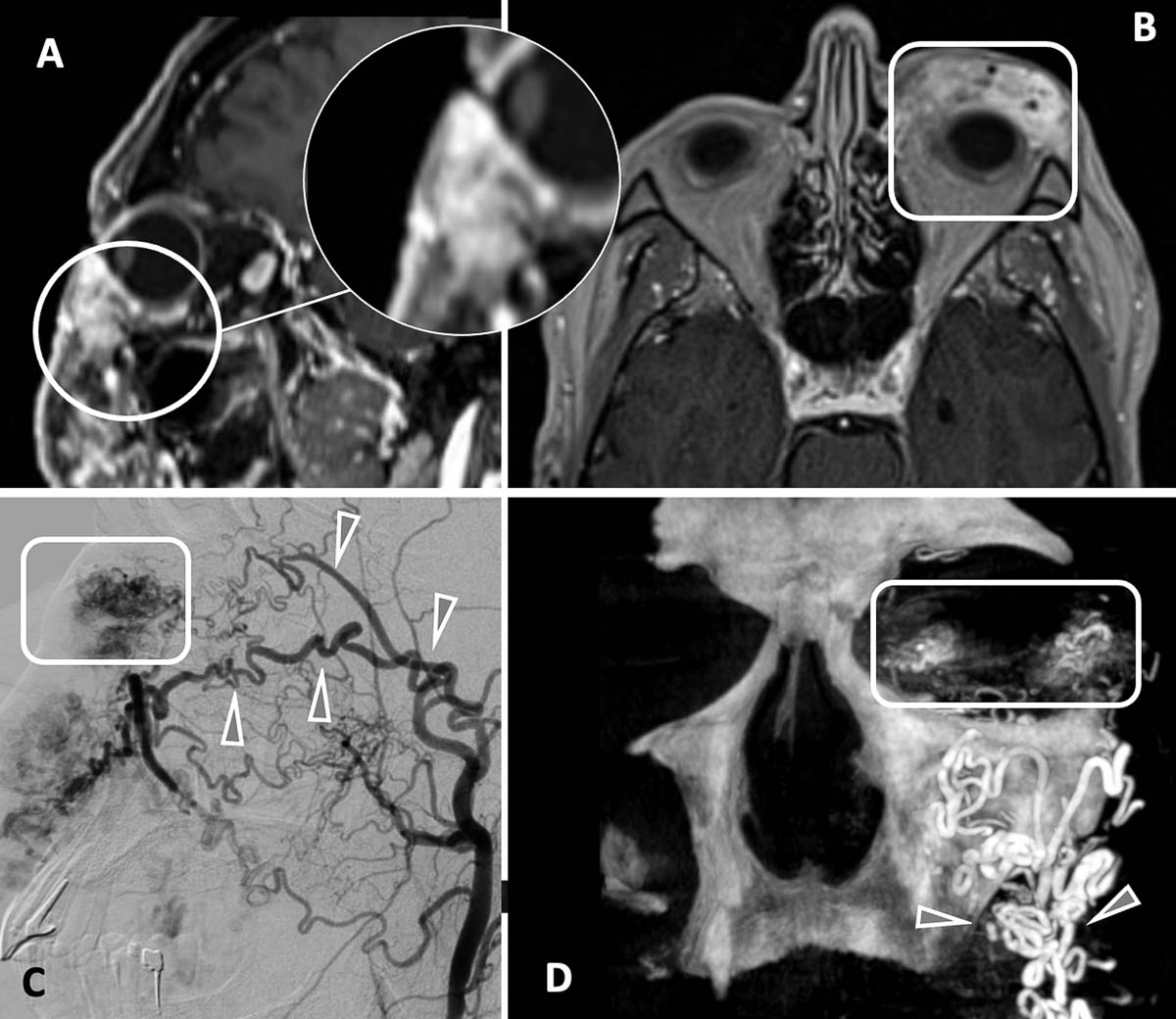
Figure 5. Patient de 50 ans, adressé pour la prise en charge d’une lésion palpébrale inférieure et jugale gauche. En IRM (A et B), on note une prise de contraste intense (rond et zoom) et des flow voids sur la séquence T1 Space FS axiale (B). L’artériographie 2D (C) montre une hypervascularisation lésionnelle et une dilatation/prolifération des artères afférentes (têtes de flèches), également bien visualisées sur l’acquisition 3D coronale (D). © Grégoire Boulouis, Denis Herbreteau
Conclusion
L’imagerie des malformations vasculaires inclut l’échographie comme examen de débrouillage et l’IRM (séquences T2 FS) pour la confirmation nosologique et comme examen préthérapeutique pour caractériser l’extension lésionnelle et l’accessibilité à des thérapeutiques invasives. L’angiographie invasive est utilisée à visée de caractérisation angioarchitecturale pour les MAV, et dans le bilan immédiatement préopératoire en sclérothérapie. Le suivi est centré sur les symptômes et la satisfaction du patient [6] et l’imagerie permet une évaluation objective de l’efficacité des traitements mis en place.











Discussion
Aucun commentaire
Commenter cet article