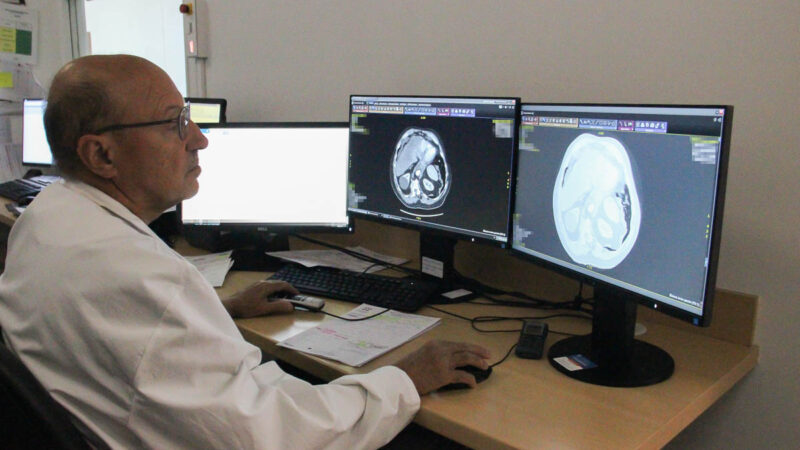
L'intelligence artificielle (IA) est de plus en plus présente dans le secteur médical et notamment en radiologie. De la détection de tumeurs à l’analyse de scanner ou d'IRM, l'IA promet d’améliorer la rapidité, la précision et l'efficience des soins. Mais selon une étude américaine publiée dans le JAMA Health Forum [1] en septembre 2025, ce progrès technologique repose sur des bases réglementaires fragiles.
Manque de transparence
Les auteurs de l'étude ont analysé 691 dispositifs médicaux intégrant de l’IA et autorisés par la Food and Drug Administration (FDA) entre 1995 et 2023, dont 76,9 % concernent la radiologie, cette spécialité comptant "le plus grand nombre de dispositifs". Ils ont constaté des problèmes de transparence et de rigueur scientifique dans les processus d’évaluation. Si la majorité des produits ont été validés via une procédure accélérée, peu d’entre eux reposent sur des données cliniques solides. "Cette étude transversale a révélé la nécessité d'améliorer la transpare








Discussion
Aucun commentaire
Commenter cet article