Recherche industrielle
Le gadoquatrane montrerait son efficacité dans des études de phase III

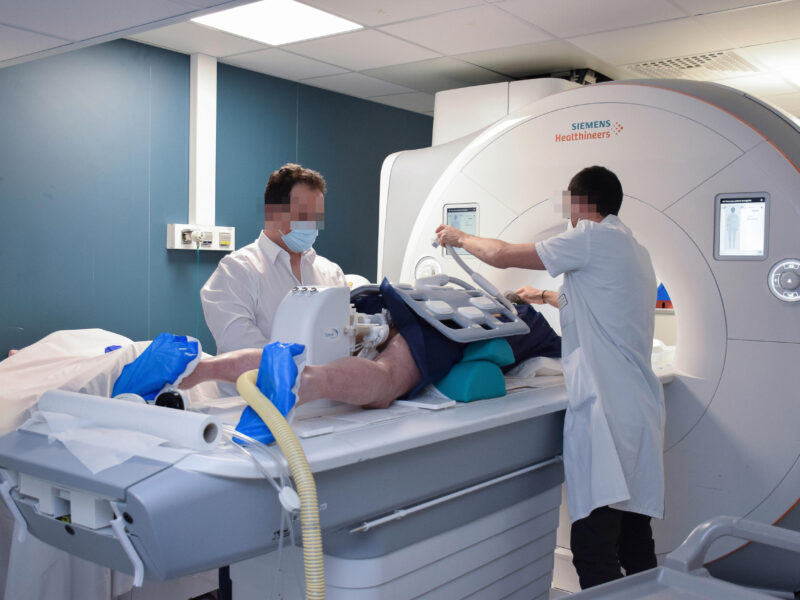
Dans les études, les chercheurs ont étudié la capacité à visualiser et à détecter des maladies connues ou suspectées utilisant le gadoquatrane (0,04 mmol Gd/kg de poids corporel) par rapport à des IRM sans injection de produit de contraste et par rapport à des IRM utilisant des produits macrocycliques dosés à 0,1 mmol Gd/kg (image d'illustration). D. R.
Il vous reste 43% de l’article à lire
Docteur Imago réserve cet article à ses abonnés
Vous avez déjà un compte ? Se connecter
- Tous les contenus « abonnés » en illimité
- Le journal numérique en avant-première
- Newsletters exclusives, club abonnés
Abonnez-vous !
Docteur Imago en illimité sur desktop, tablette, smartphone, une offre 100% numérique
23 €
par mois







Discussion
Aucun commentaire
Commenter cet article