Omniscan® et Magnevist® quittent les étals. Dans une lettre envoyée ce 12 janvier 2018, l’Agence nationale de sécurité du médicament (ANSM) informe les professionnels de santé que les autorisations de mise sur le marché de ces deux produits de contraste pour IRM sont suspendues à compter du 15 janvier. Ce faisant, elle relaie pour la France une décision de la commission européenne en date du 23 novembre, prise sur recommandation de l’Agence européenne du médicament (EMA).
Des dépôts dans le cerveau
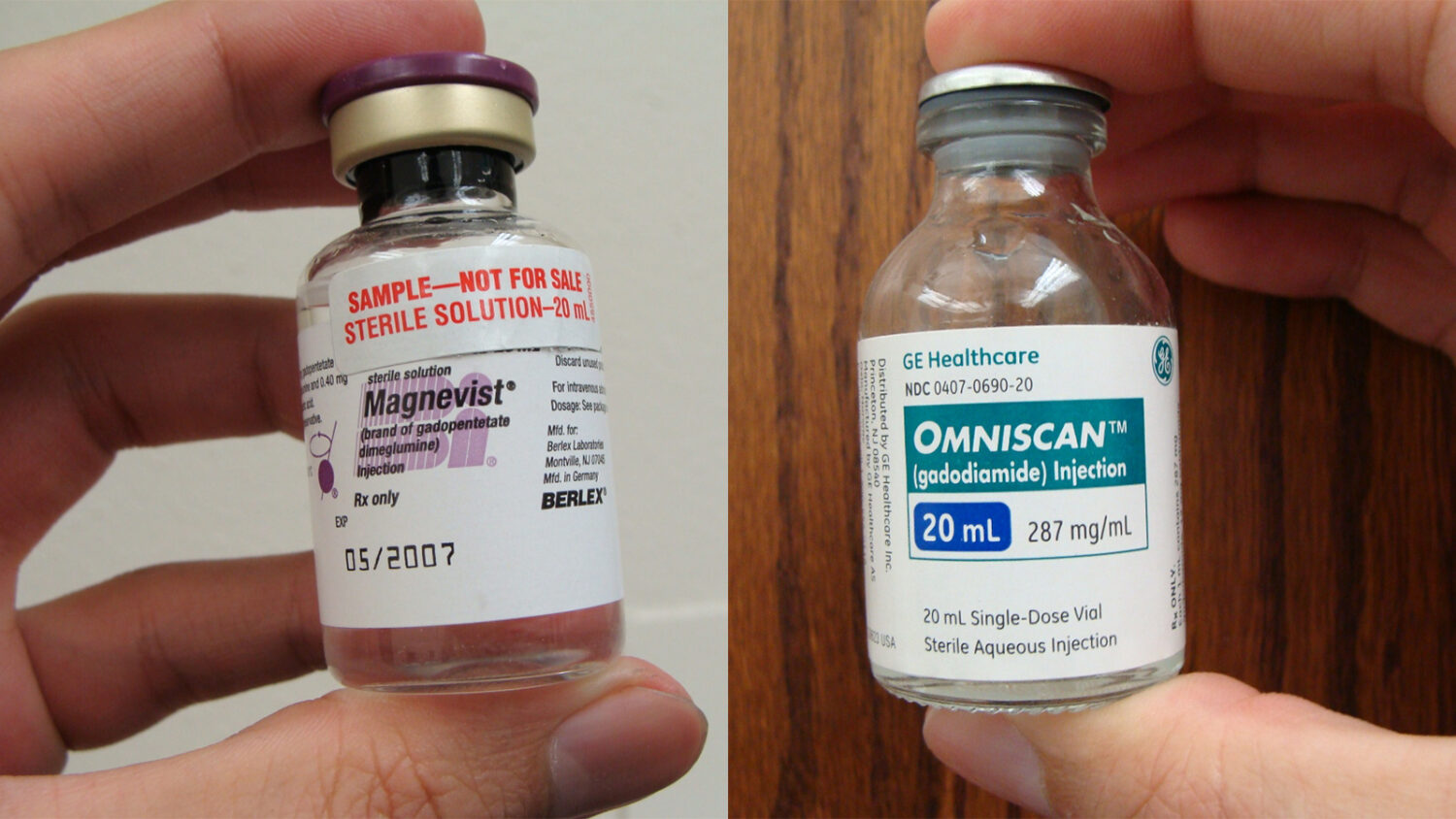
Omniscan® est le nom commercial du gadodiamide, vendu par GE Healthcare ; Magnevist® est celui de l’acide gadopentétique, du laboratoire Bayer. Il s’agit de produits de contraste à base de gadolinium de type linéaire. L’EMA motive leur mise à l’écart par leur tendance à se déposer dans le cerveau après des injections multiples. « Une revue exhaustive […] a conclu à la rétention de gadolinium dans le cerveau à la suite de l’utilisation de produits de contraste à base de gadolinium par voie intr










Discussion
Aucun commentaire
Commenter cet article