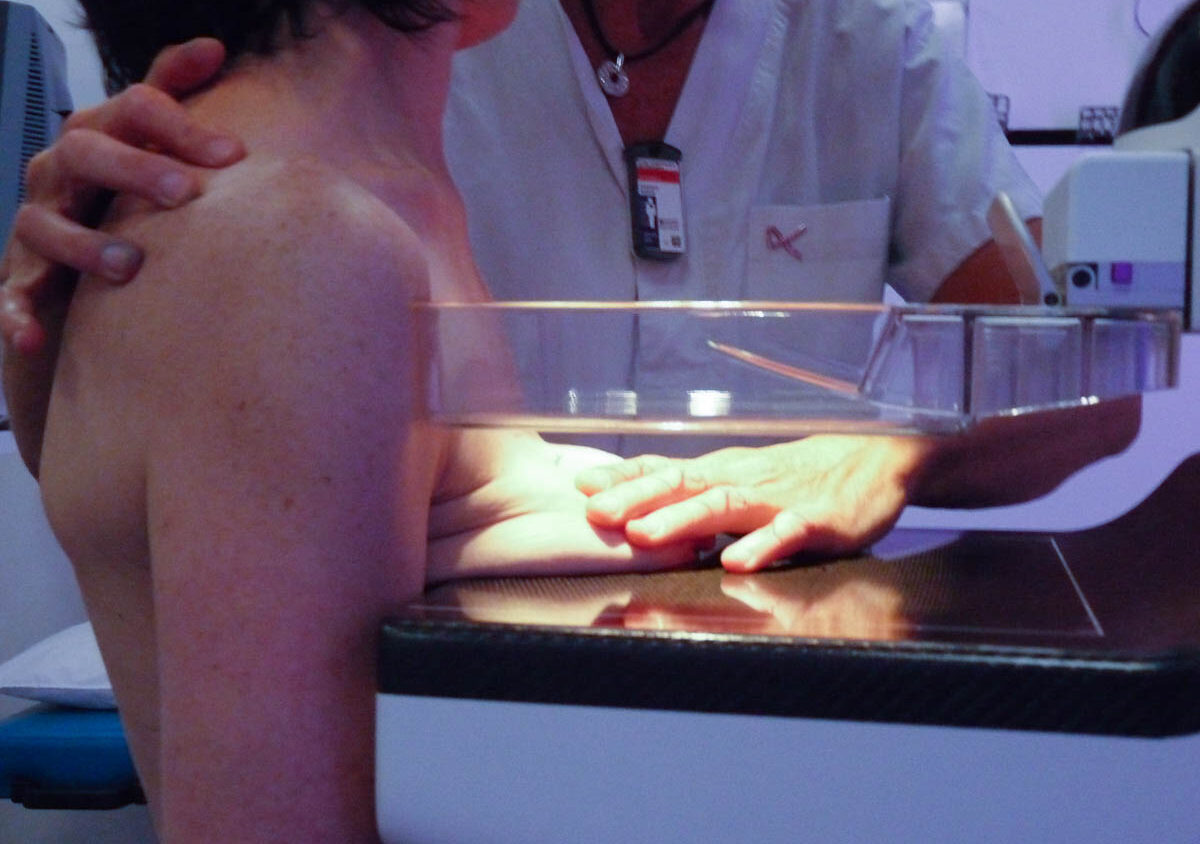
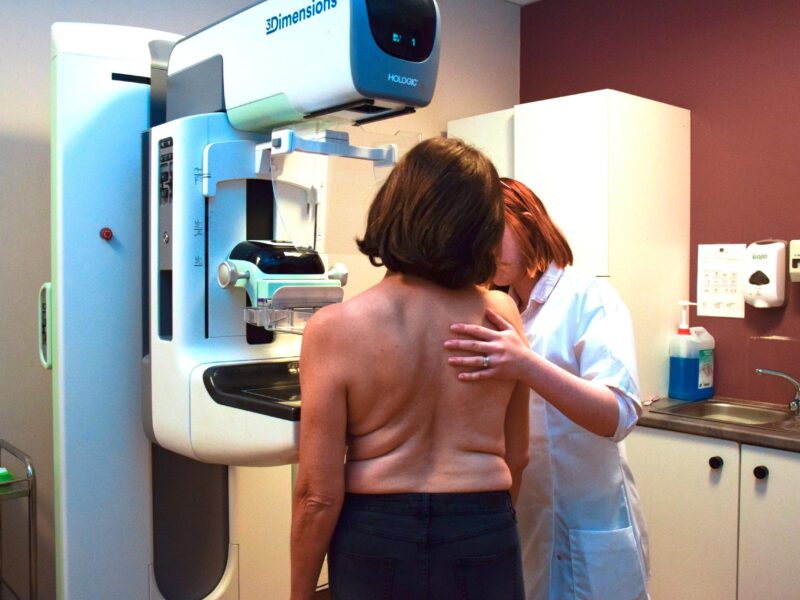
Le dépistage organisé du cancer du sein en France a subi une modification. Désormais, les textes réglementaires prévoient que les équipements soient exclusivement numériques. Dans un arrêté publié le 9 mars 2019 dans le Journal Officiel, il est indiqué que « seules les installations de mammographie numérique sont autorisées à participer au programme de dépistage. »
Une sous-détection des cancers par les mammographes analogiques
Jusqu’ici, les textes indiquaient que « dans l’état actuel des connaissances scientifiques, seuls les mammographes analogiques, avec films à surface argentique, sont autorisés à participer au programme de dépistage. » Cette disposition a été supprimée au profit du numérique.
L’institut national du cancer précise que cette décision s’appuie sur une évaluation qu’il a réalisée en décembre 2018. Celle-ci démontrait « une sous-détection des cancers par les mammographes analogiques [et] les mammographes numériques CR de marque Konica Minolta ».









Discussion
Aucun commentaire
Commenter cet article