Introduction
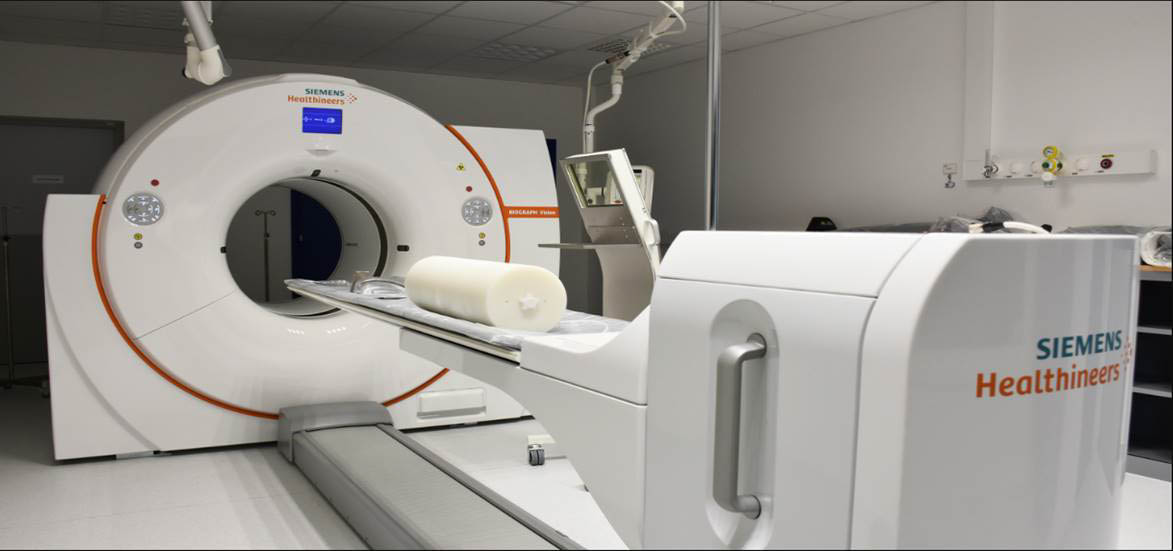
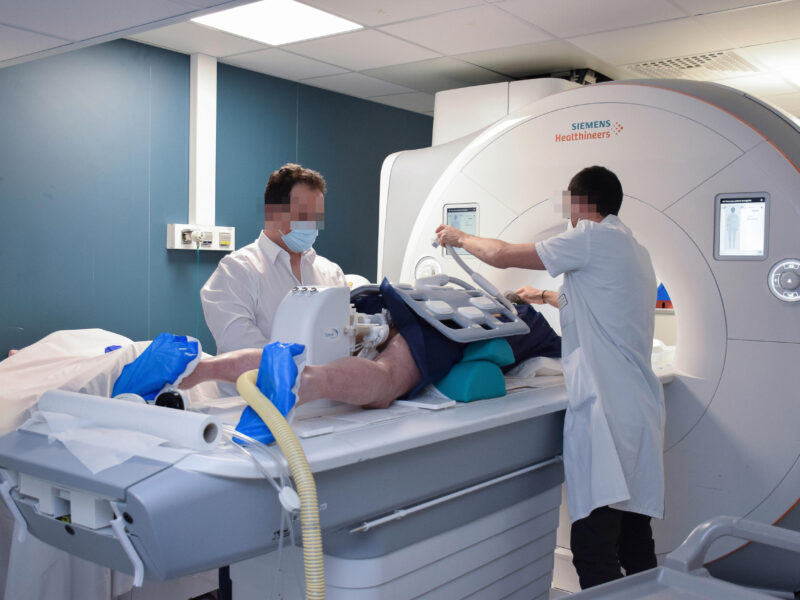
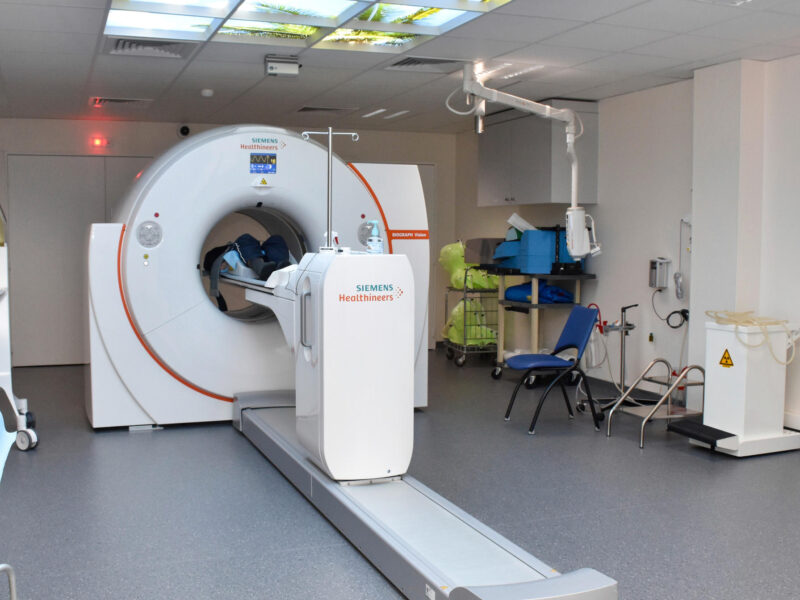
La TEP-IRM est une technique d’imagerie multimodale permettant de combiner une imagerie TEP (tomographie par émission de positons) et une imagerie par résonance magnétique (IRM). C’est une technique émergente, puisqu’en mai 2021, la TEP-IRM nantaise était la cinquième installation en France, au sein du centre IMageRie moléculAire Multimodale (IMRAM) du CHU de Nantes (figure 1). L’activité de la TEP-IRM en cardiologie représente environ 20 % de l’activité totale en clinique et en recherche.
Compte tenu de sa multimodalité, cette imagerie demande une double, voire une triple expertise pour son interprétation, alliant les compétences à la fois du radiologue, du médecin nucléaire et, à Nantes, du cardiologue. Sa réalisation nécessite une équipe de manipulateurs entraînée à l’imagerie cardiaque.
Cet article dressera un état des lieux de la TEP-IRM en cardiologie en 2023 à partir de l’expérience nantaise. Il rappellera les techniques de réalisation, son interprétation








Discussion
Aucun commentaire
Commenter cet article