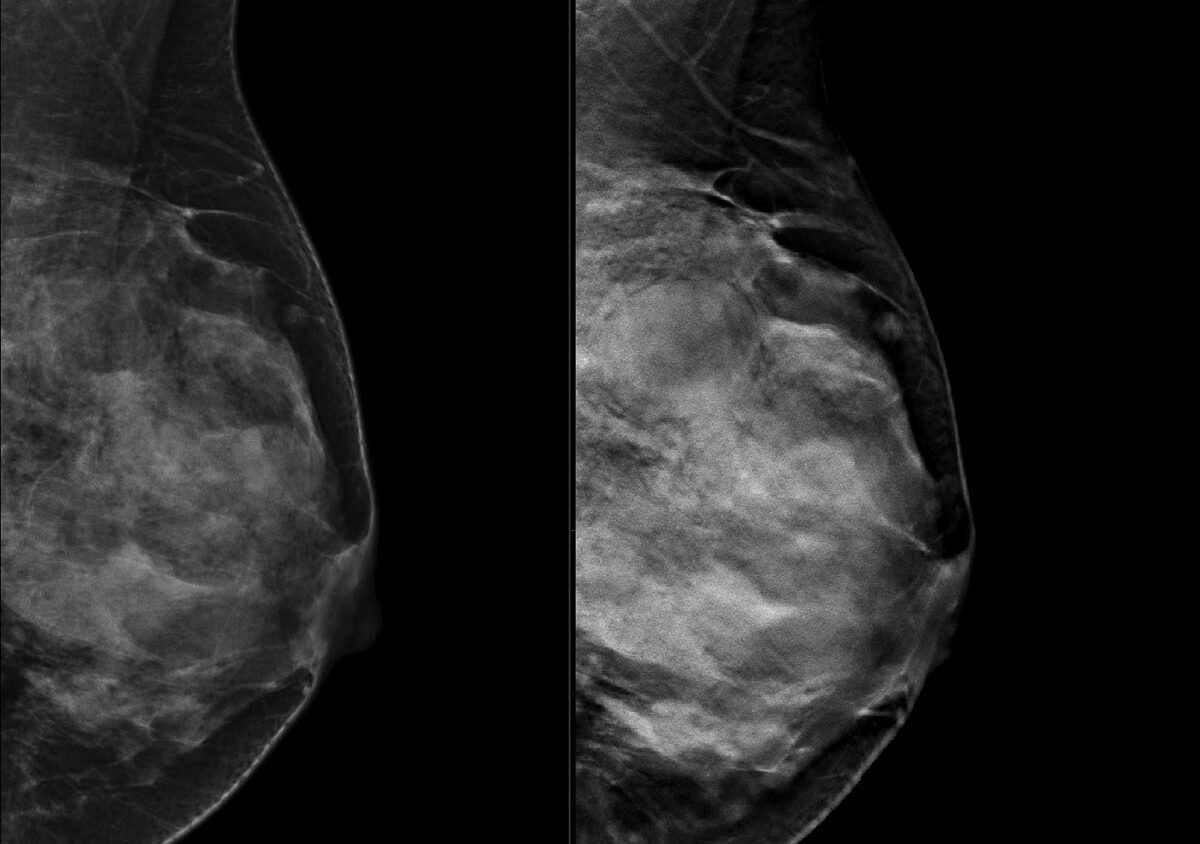
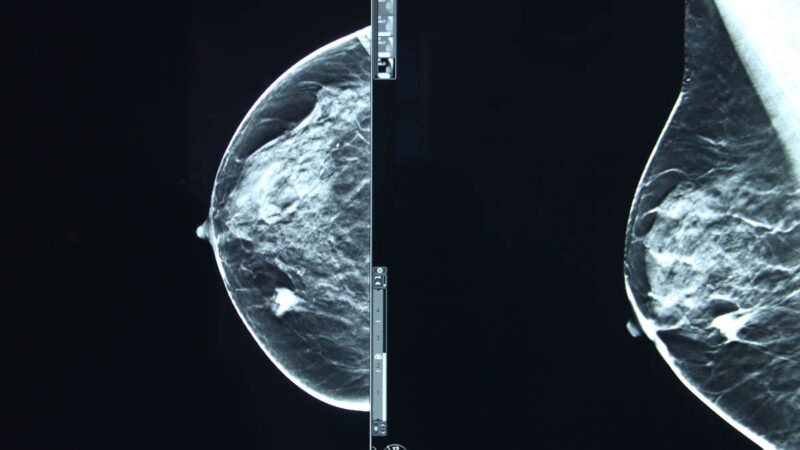
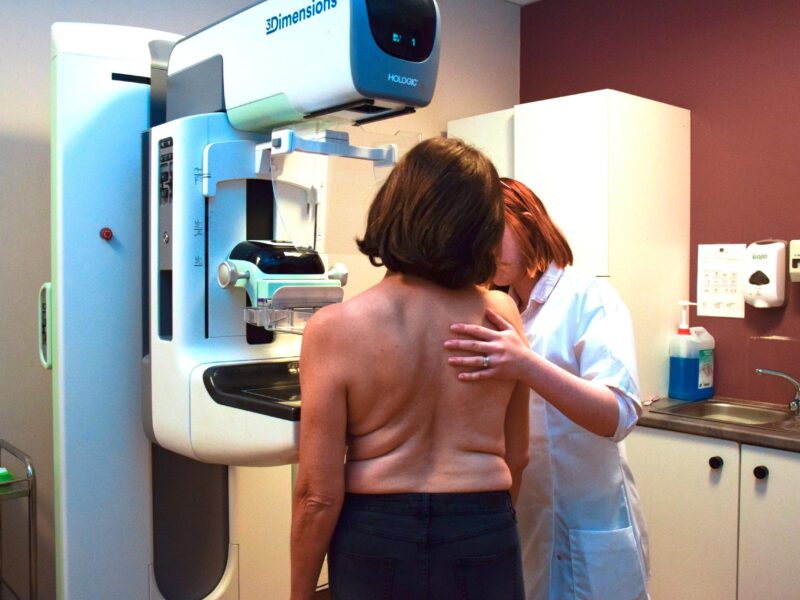
La tomosynthèse pourrait-elle être intégrée au dépistage organisé du cancer du sein ? La HAS s’est interrogée sur cette éventualité et vient de publier le fruit de ses investigations dans le premier volet de sa revue critique de la littérature sur la performance de la tomosynthèse.
Des études passées au crible
Ces travaux, réalisés à la demande de l‘Institut national du cancer (INCa) et de la Direction générale de la santé (DGS), ont abouti à un premier rapport de 163 pages que la HAS décrit comme « une étape préliminaire à l’évaluation de la pertinence, la faisabilité, la sécurité et l'efficience de l’intégration possible de la tomosynthèse dans le dépistage organisé ». Pour élaborer son rapport, la HAS a passé au crible la littérature disponible sur la période 2012-2019 dans plusieurs banques de données bibliographiques. Elle a notamment analysé des méta-analyses, des études françaises et européennes, des revues critiques de la littérature, ainsi que des rapports d’agence d’évaluation










Discussion
Aucun commentaire
Commenter cet article