À l'occasion de la première journée d’imagerie du cancer du sein de l’institut Curie, le 6 septembre 2023 à Paris, Romain-David Seban, médecin nucléaire de l'institution sur le site de Saint-Cloud (Hauts-de-Seine), a pris la suite de sa consœur Virginie Huchet pour évoquer trois traceurs de TEP innovants particulièrement intéressants dans le cancer du sein. « Le traceur de référence est le [18F]-FDG. Toutefois, ce dernier manque de spécificité. À l'ère de la médecine de précision, nous avons besoin de nouveaux traceurs », a-t-il affirmé en introduction.
Trois traceurs innovants
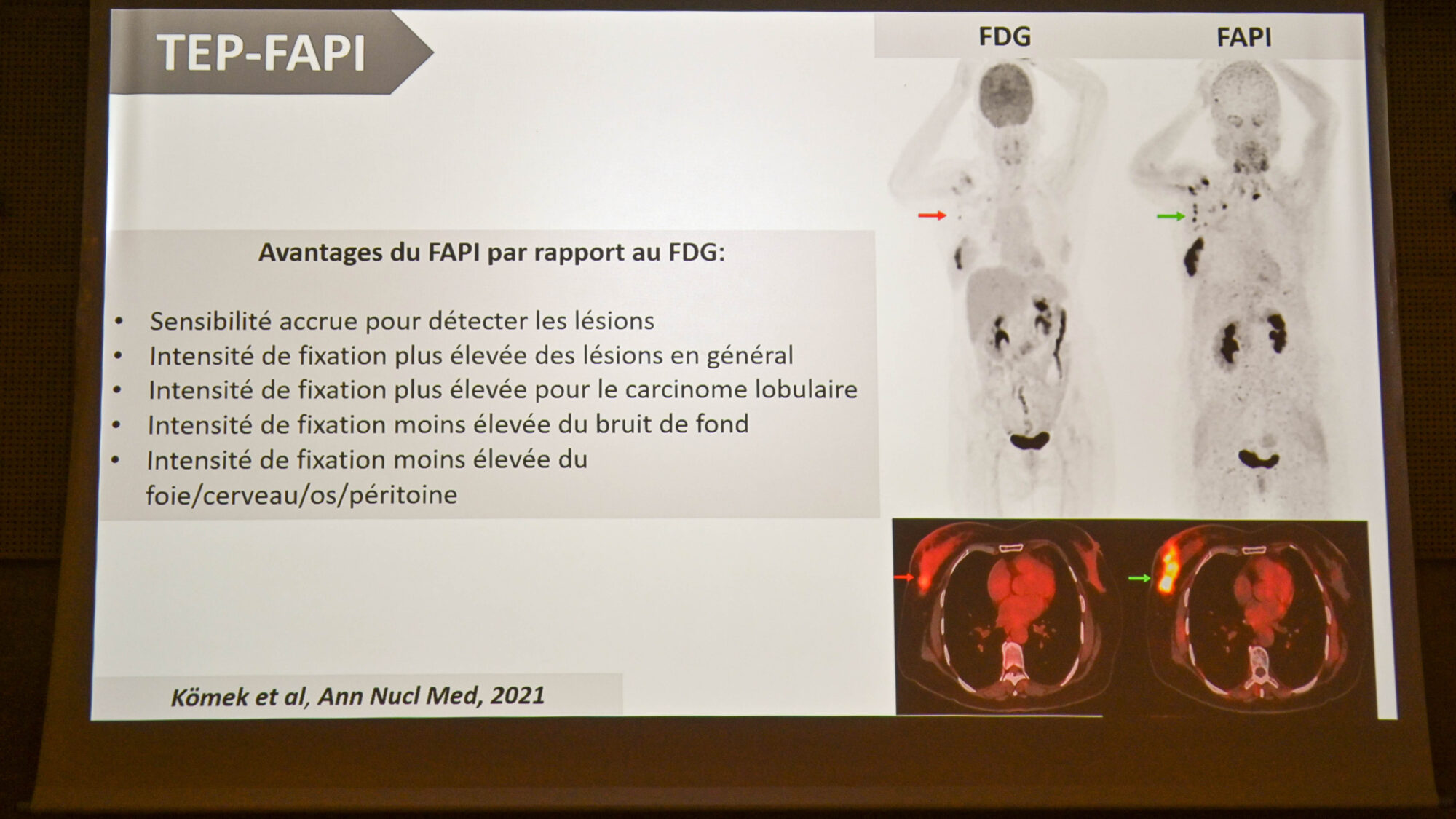
Romain-David Seban a présenté tour à tour trois traceurs par ordre de stade de développement : le [18F]-FES (fluoroestradiol) ciblant les récepteurs à l'œstrogène, seul à bénéficier d'une AMM, le FAPI, ciblant des protéines en surface des fibroblastes associés au cancer, et les anticorps et afficorps anti-HER2 ciblant la protéine HER2.
« On observe une fixation hépatobiliaire très élevée »
Le plus établi de









Discussion
Aucun commentaire
Commenter cet article